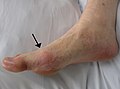
痛風
| 痛風 | |
|---|---|
 尿酸 | |
| 分類および外部参照情報 | |
| 診療科・ 学術分野 | リウマチ学 |
ICD-10 | M10 |
ICD-9-CM | 274.0 274.1 274.8 274.9 |
| OMIM | 138900 300323 |
| DiseasesDB | 29031 |
| eMedicine | emerg/221 med/924 med/1112 oph/506 orthoped/124 radio/313 |
| Patient UK | 痛風 |
| MeSH | D006073 |
痛風(つうふう、gout)とは、尿酸が体内で析出して結晶ができることにより、関節炎などを来たす疾患である。背景には高尿酸血症などが存在する。
目次
1 日本語の名称
2 原因
3 症状
4 疫学
5 検査
6 治療
6.1 対症療法
6.1.1 好中球の活動抑制
6.1.2 消炎・鎮痛
6.1.3 患部の管理
6.1.4 緩やかな尿酸の排出
6.1.5 尿酸値上昇要因の排除
6.1.5.1 食事療法
6.2 予防
6.3 その他
7 遺伝
8 民間療法と喫茶の歴史
9 参考文献
10 関連項目
11 外部リンク
日本語の名称
この疾患の「痛風」と言う日本語名の由来には、幾つかの説が存在する。まず、痛みが起こる場所(発作の箇所)が、まるで風が吹くように足・膝・腰・肩・肘・手・胸骨など、全身の関節や骨端部を移動し、なおかつ、風が強くなったり穏やかになったりするように痛みが酷くなったり和らいだりを繰り返すことから命名されたという説がある。他に、痛みの悪風に中る(あたる)という意味で「痛風」となったとする説や、痛み発作が出ている部分は吹いてきた風が当たるだけでも痛いから「痛風」となったとする説もある。
原因

関節液の尿酸結晶
ヒトを含むヒト科は、進化の過程で尿酸オキシダーゼを失ったため、プリン塩基を処分する時、体内では尿酸にまでで処理が止まってしまい、尿酸よりも水溶性が高いアラントインへの変換は、一部が体内で発生した活性酸素種によって非酵素的に進む程度である[1]。
尿酸は水溶性が低いため、体内に蓄積すると、特に体温の低い末梢部で体液に溶け切れなくなった尿酸が析出しやすい。析出して結晶化した尿酸は、炎症を引き起こして痛風発作を誘発する[2]。
高尿酸血症の患者にきっかけが加わると痛風を発症する。何がきっかけなのか明確ではないことも多い。
健康状態における人体の血中には、ごく普通に尿酸が含有されているが、この濃度(血中尿酸値)が何らかの理由により著しく上昇すると、本来人体が持つ恒常化機能を超えて飽和解消できず、特に体温が低い足部などにおいて、尿酸が溶解しきれずに尿酸塩として結晶化して関節包内などに付着することが知られている。この状況においては、白血球群のうち、特に好中球が尿酸結晶を攻撃(捕食活動)を行うことが知られている。
好中球による尿酸結晶捕食活動が激化すると、その活動による過大なエネルギーや、尿酸を抱え込んで死亡した好中球の遺骸そのものによる影響などから、血管壁がダメージを受けて大きな炎症を発生する。当然に、当該部位周囲の神経組織をも相当に刺激し、患者は「内側からの激痛」を感じることとなる。
また、血中含有尿酸の濃度が急激に低下した場合においても、痛風発作が生じることが知られている。これは、好中球が攻撃対象である尿酸結晶の行方を急激に見失うと、対象を探し続けて活動を激化させることによるためとも言われているが異論も多く、血中尿酸値急降下時の明確な発作システム自体の解明はなされていない。ただし後述の通り、疫学的には、血中尿酸値の上昇とともに血中尿酸値の急降下も、痛風発作の要因であることは広く知られており、痛風発作時における尿酸生成阻害剤や尿酸排出促進剤などの服用は禁忌とされていることが多い[要出典]。
必ずしも恒常的な高尿酸血症患者がすべて痛風発作を起こすわけではなく、そのメカニズムは解明しきれていないが、よく知られている発作のきっかけとしては、脱水症状に伴う急激な尿酸値の変動、物理的衝撃による結晶の剥落、不適切なタイミングでの尿酸コントロール薬の投与、激しすぎるスポーツなどが考えられている。アルコールの痛飲はアルコール代謝に水が回ることで起こる脱水症状に加え、乳酸と尿酸の競合による尿酸排出の遅れによって尿酸値を激しく変動させ、翌日朝に痛風を起こすきっかけとなることが多いともされる。
あくまで、高尿酸血症の患者でも痛風を起こさないケースは少なくないため、引き金となる要因が全て分かっているわけではない。米国で、高尿酸血症の患者に尿酸値を下げる薬を処方しないのはその考え方に基づいているが、高尿酸血症は腎臓結石など別の病気のリスク要因であることは忘れるべきではない。
血清尿酸値に影響を及ぼす比較的頻度の高い遺伝子としてURAT1 (SLC22A12) が知られていたが、GWAS(ゲノムワイド関連解析)により大規模に発見された。即ちSLC11A9, SLC2A9, SLC17A1, SLC22A12, SLC22A11, SLC16A9, ABCG2, LRP2, PDZK1, GCKR, TRIM46, INHBB, INHBC, SFMBT1, TMEM171, VEGFA, BAZ1B, STC1, PRKAG2, HNF4G, A1CF, ATXN2, UBE2Q2, IGF1R, NFAT5, MAF, HLFなどである。これらの遺伝子は一般の痛風の発症に関係していると考えられる。この中でSLCのつくものはATP結合カセットを持たないトランスポーター(輸送蛋白質)であり、腎臓の尿細管に分布し尿酸の尿中排泄に関係すると考えられる。ABCG2は主として腸管に分布し、腸からの尿酸排泄の低下により高尿酸血症を来し、痛風を来す事が示唆されている[3]。この他、痛風になりやすいヒトは、アセトアルデヒド脱水素酵素に特定の変異を持っているとする研究結果も存在する[4]。
症状
関節に激烈な痛みが起こり、発赤や発熱を伴う。尿酸の結晶は比重が高く重力に引かれて足部に沈着しやすいため、痛風発作(痛風性関節炎)は足趾(特に母趾MP関節)に好発する。初発症状は足部であることが多いが、足関節、膝関節から発症することもある。足の親指の付け根やアキレス腱部分などに発作が起きると痛みだけでなく歩行困難になり、まともに歩けるようになるまで1か月ほどかかる場合もある。その点は骨折や捻挫と同じである。発作を繰り返すたびに症状は増悪する。発作の痛みは骨折の痛み以上といわれ、非常に苦痛を伴う。また、耳介などに痛風結節と呼ばれる皮下結節を作ることがあり、これが診断の助けとなる。X線では骨髄腫のようにpunched out(打ち抜き)と呼ばれる骨破壊像が見える。痛風と鑑別を要する関節炎の疾患としては関節リウマチ、変形性関節症、偽痛風がある。
痛風によりMP関節にできた関節炎
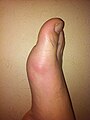
痛風の炎症部位

耳介にできた痛風結節
疫学
患者の90%以上が男性。最近の疫学的研究によると、アルコールは肝臓で尿酸が作られるのを促進し、尿酸濃度をあげてしまうため、痛風のリスクを高める。特にビールは最もリスクが高く[5]、ワインは飲んでも痛風のリスクを高めない[6]ほか、焼酎やウイスキーもそれほど痛風のリスクは高くはない(なおアルコール飲料自体のプリン体は、食品の中でも比較的少ない方である)。尿酸とはプリン体と呼ばれる物質の代謝産物であり、プリン体を多く摂取すると高尿酸血症、さらには痛風の引きがねとなると考えられる。肉のみならず魚に含まれるプリン体も痛風のリスクを高めるが、野菜に含まれるプリン体(麦芽[7]、豆類に多い)は高めない[8]。また、フルクトース(果糖)は急速に代謝されてアシドーシスを引き起こしやすく[9]、酸性下で尿酸が析出しやすくなる。フルクトースを構成体に持つ砂糖の多いドリンクを週に5~6杯飲む場合やフルクトースを含むフルーツジュースの摂取も痛風のリスクを増大させる[10]。近年、高尿酸血症に関わる遺伝子が各国(含日本)で発見されている。
そのほか、精神的ストレスや水分摂取の不足も発症の引きがねとなる。特に水分摂取の不足に関しては、日常的に意識して水分を多めに取り、血中尿酸濃度を(排尿によって体外に出す事で)低く保つことが勧められている。
2018年(平成30年)10月10日付けのBMJ誌電子版に、ニュージーランドオタゴ大学のTanya J Major氏らは、食事の内容は血清尿酸値に影響は与えるが、一般集団の血清尿酸値の変動に対する食生活の寄与は、遺伝的な要因に比べると遙かに小さかったとする報告を掲載した。[11]
検査
- 痛風を発症する患者では、少なくとも非発作時には血液検査での高尿酸血症が見られるが、25%の患者で発作時に尿酸値が正常である。
- 関節穿刺液検査における多形核細胞の増加と尿酸結晶の証明(これが一番大事だが、感度は100%ではない。85%程度とする文献がある)。
治療
対症療法
好中球の活動抑制、抗炎症薬の投与、鎮痛薬の投与、患部の管理、緩やかな尿酸の排出、尿酸値上昇要因の排除、の5手法併用を以って行う。
好中球の活動抑制
コルヒチン製剤力価0.5mgを、発作を起こすに足る程度の好中球の活動の抑制が果たされるまで、概ね4時間以上の間隔で経口投与することが多い。- 日本において認可されているコルヒチン剤は製品名「コルヒチン」として塩野義製薬が生産していたが、2010年4月に高田製薬に販売が継承された。国内では先発品の本剤しかないが、薬価が安いことがあり、ジェネリック品は開発されていない。海外においてもインガラボラトリ社(インド)の製品名「ガウトニル」など対外向けジェネリック産品が生産されているが、日本においては未認可である。
消炎・鎮痛
現状では、非ステロイド系鎮痛消炎薬を使用することが多い。例えば、力価60mgのロキソプロフェンナトリウム製剤を、その投入が不要と認められるまで、概ね8時間以上の間隔で経口投与することが多い。ロキソプロフェン製剤服用にあたっては、胃壁へのダメージを避ける目的で、テプレノン製剤・レバミピド製剤などの胃粘膜保護剤を併せて処方することが多い。
NSAIDs(非ステロイド系抗炎症鎮痛薬)と呼ばれる種類の痛み止めの薬で対症療法を行う。インドメタシンなどに、臨床研究に基づく科学的根拠がある(根拠に基づく医療)。- 疼痛が強い患者では、ステロイドの全身投与や、単関節炎患者では関節内投与が極めて有効である。最近では、最初にNSAIDsではなくステロイドを服用したほうが、効果は同等で副作用(悪心、消化管出血など)は少ないとする報告がある[12]。
患部の管理
- 発作を起こしている関節ないし周辺部位は、安静および冷涼に保持する必要があり、患部を動かしたり熱温する行為は炎症を重篤化させることが知られている。特に、発作時患部の駆動および温度上昇の双方を同時にもたらす入浴は禁忌とする。患者が、安易に民間療法的な発想で、痛風発作と同様に関節部に痛みを伴う関節リウマチの慢性期療法等の温泉療法を連想し入浴を行うと、痛風発作の症状をほぼ100%悪化させる。
緩やかな尿酸の排出
- 体内の尿酸を自然に排泄する手段として、水分を多めに摂り排尿を促す。
クエン酸製剤であり尿アルカリ化薬であるウラリットが尿酸の排出を促し、痛風を緩和するとされている[13]。- 尿酸排泄促進薬の使用中は酸性尿となるため尿路結石や腎障害を発症しやすく、尿アルカリ化薬を併用する。
- 痛風発作中に尿酸降下薬の投与を開始すると発作を増悪させるので、投与を開始してはならない。ただし尿酸降下薬の投与中は原則として服用を中止しない。
尿酸値上昇要因の排除
- 血内の尿酸を濃化させる行為を慎む。具体的には、業務・対人などストレスを発生させる行為の中止、負荷のかかる運動の中止(負荷のかかる運動によって死滅した筋細胞はプリン体の主要な供給源のひとつである)、プリン体を多く含む食材の摂食中止、飲酒の中止などを行う。
食事療法
- 高尿酸血症・痛風の治療ガイドラインの「生活指導」では、特に「1日400mgを目安にしたプリン体の摂取制限」が示されている[14]。
そこら
予防
高尿酸血症患者においては、その治療方法そのものが、すなわち痛風発作の予防方法のほぼ全てを充足するほか、非高尿酸血症者においても、日常において血中尿酸の急激な濃淡を起こさないような体調・ストレスの管理を要する。
- 尿酸産生抑制剤であるアロプリノールやフェブキソスタット・トピロキソスタット、尿酸排泄促進剤であるベンズブロマロン(分泌後再吸収阻害剤)、プロベネシド(分泌前再吸収阻害剤)[15]を予防的に経口投与し、高尿酸血症を改善する。これらは、高尿酸血症の原因が、尿酸産生過剰によるものか尿酸排泄能力低下によるものか、あるいは薬効の患者への影響度などを見極めて使い分ける。
- 血中尿酸値の濃化・淡化を問わず、その急激な変動そのものが痛風発作の原因となるため、これらの薬剤については、急激な尿酸値低下による発作の悪化や再発を誘引せぬよう、痛風発作の発現中ならびに寛解直後数週間の服用は推奨されていない。
- 『高尿酸血症・痛風の治療ガイドライン』[16]では、「適度な量の飲酒」、「プリン体の摂取を控えめにする」、「十分な水分摂取」、「尿をアルカリ性に保つ」、「運動」、「ストレスの解消」がすすめられている。
帝人ファーマが創製し、同社が日本で、イプセンがヨーロッパで、TAP社、(後に武田薬品に買収される)が米国で開発したフェブキソスタットが新規痛風治療薬として米国では2009年、日本では2011年にフェブリク®(帝人ファーマ製造販売)として承認された。
富士薬品が創製したトピロキソスタットが、2013年よりトピロリック®(富士薬品)/ウリアデック®(三和化学研究所)の2ブランドで販売されている。
その他
痛風患者は発作の前兆を感じることがあると言われ、そのときコルヒチンを飲むと発作を予防する効果があるとされている。しかしこの治療法に臨床研究に基づく根拠はない。ただし、発作の初期症状である発作発現部に感じる「違和感」や、ごく軽い内部から感じる痒み等については、痛風発作の初発患者のほとんどがこれを軽微な思い過ごしと見過ごして発作を激痛による歩行困難となるまで重篤化させるが、再発患者は既にその初期症状の特徴である患部の微妙な違和感を体験しているため、痛風発作発生のごく初期にいち早く診療を受けてコルヒチンを処方され服用して、激痛が発生する前に発作の進行を抑制・寛解させるケースが非常に多い。これは、痛風発作の激痛に懲りた経験のある患者にとって再度くりかえし過酷な発作を蒙りたくないと考えるゆえの当然の行動によるものであり、あくまで発作歴のある患者が発作初期の患部の違和感を素早く感知して早期に対症療法を受けたことによる成果であって、「前兆」「予感」等ではなく発作の「自覚症状」にもとづくものであり、その診療経緯は当然に診察医のカルテにも記録されるので、疫学的に反映させることが可能なものである。
遺伝
痛風を来す作用が極めて強く、1つの遺伝子が痛風の原因となる場合(単一遺伝子病)と、1つの遺伝子の作用が弱く、複数の遺伝子と環境要因が加わって痛風を来す場合(多因子病)がある。前者にはPRPP合成酵素亢進症、HPRT欠損症(レッシュ・ナイハン症候群)などの酵素異常症、ウロモデュリン異常症などがある。後者には多数の遺伝子があり、上記のように少なくとも27個の遺伝子が関係している。
民間療法と喫茶の歴史
水分を多めに摂る事で、非常な痛みを伴う症状の発生を予防できる事は、古くから経験によって知られていた。これは排尿によって血中尿酸濃度を下げる効果があるため、関節への尿酸結晶の発生を避けられるためである。
特に利尿作用のある緑茶・紅茶・コーヒー等を多量に摂取して大量に排尿すれば、それだけ大量の尿酸が体外に排泄される事にも繋がるため、より症状発生の予防ができるとされている。しかし利尿作用も度が過ぎると、脱水症状を起こして症状が悪化したり、尿路結石が出来る可能性もある。
ヨーロッパに喫茶の習慣が伝えられると、痛風の症状を緩和できたり予防できるとして、盛んに喫茶が流行・奨励された。
なお当時の緑茶が、日本・中国などのアジアでしか生産されていなかった事もあり、大変贅沢な療法とされ、オランダが日本産や中国産の、イギリスが中国産の緑茶を独占的に扱っていたため、緑茶が高価過ぎて手が出せない事情から、フランスやドイツでは、コーヒーの飲用が流行したという。紅茶は、保存に便利で効果の程は緑茶と大きく変わらないとして、後々のイギリスにおける紅茶文化発展の元となった。
クエン酸製剤が痛風緩和に有効である[13]ことが医学的に証明されている。従ってクエン酸を多く含むレモン、グレープフルーツ、梅干、トマトなどの摂取が痛風対策に有効であることになる。[要出典]
また、尿酸値を下げることが発作のリスクを抑えるという観点から、肝機能向上(中性脂肪を減らし、肝臓内に蓄えられているプリン体自体を減らす)と腎機能向上(腎臓の負担を減らし、効率的に尿酸の排出をうながす)は重要な療法といえる。具体的には、散歩などの有酸素運動、低塩分、低カロリーな食事、カリウムを多く含む食品の摂取、十分な水分補給と入浴、睡眠などが効果があるとされる。
アメリカにおいて尿酸値を下げる効果と痛風発作の痛みを緩和する効果があると広く信じられているアメリカンチェリーは、アントシアニンなどのポリフェノール類が働いているといわれている。一方、アメリカ食品医薬品局 (FDA) は、痛風への効能を謳ってチェリー加工品を販売する業者に対し、証明されていない効能をラベルに載せるのをやめるよう警告している[17][18]。
経験的な民間療法として、スライスした生たまねぎを半分から一個分、水にさらさずに食べることにより、発作時の劇的な痛みを軽減し、また痛みの続く期間を短くするという説がある。また、日常的に摂取することにより、発作を抑え、痛風体質の改善にも高い効果があると言われている。これは、たまねぎに多く含まれているクェルセチンの炎症抑制効果と、尿酸の増加を抑制する効果のためではないかと言われている。ただし、生のたまねぎの摂取は、体質によって胃が痛むなどの副作用もあり、この点には注意が必要である。
参考文献
^ 尿酸の酸化作用と抗酸化作用
^ 高木和貴、上田孝典「尿酸分解酵素PEG化ウリカーゼの適応と意義」『高尿酸血症と痛風』18(2), 2010, pp. 41-46
^ Kimiyoshi Ichida; Hirotaka Matsuo, Tappei Takada, Akiyoshi Nakayama, Keizo Murakami, Toru Shimizu, Yoshihide Yamanashi, Hiroshi Kasuga, Hiroshi Nakashima, Takahiro Nakamura, Yuzo Takada, Yusuke Kawamura, Hiroki Inoue, Chisa Okada, Yoshitaka Utsumi, Yuki Ikebuchi, Kousei Ito, Makiko Nakamura, Yoshihiko Shinohara, Makoto Hosoyamada, et al. (2012年). “Decreased extra-renal urate excretion is a common cause of hyperuricemia.”. Nature Communications 3. doi:10.1038/ncomms1756. PMID 22473008. http://www.nature.com/ncomms/journal/v3/n4/full/ncomms1756.html.
^ Identification of rs671, a common variant of ALDH2, as a gout susceptibility locus
^ Choi HK; Atkinson K; Karlson EW; Willett W; Curhan G. Alcohol intake and risk of incident gout in men: a prospective study. Lancet 2004 17;363:1277-81.
^ Choi HK; Atkinson K; Karlson EW; Willett W; Curhan G. Alcohol intake and risk of incident gout in men: a prospective study. Lancet 2004 17;363:1277-81.
^ KIRIN_お問い合わせ プリン体と人体の関係について (参考)
^ Choi HK; Atkinson K; Karlson EW; Willett W; Curhan G. Purine-rich foods, dairy and protein intake, and the risk of gout in men. NEJM. 2004 11;350:1093-103.
^ 高橋隆一 高カロリー輸液施行中に認められるアシドーシス
^ Hyon K Choi, Gary Curhan. Soft drinks, fructose consumption, and the risk of gout in men: prospective cohort study BMJ 2008; 336: 309-12.
^ Merriman, Tony R.; Dalbeth, Nicola; Topless, Ruth K.; Major, Tanya J. (2018年10月10日). “Evaluation of the diet wide contribution to serum urate levels: meta-analysis of population based cohorts” (英語). BMJ 363: k3951. doi:10.1136/bmj.k3951. ISSN 1756-1833. PMID 30305269. https://www.bmj.com/content/363/bmj.k3951.
^ Man CY et al. Comparison of oral prednisolone/paracetamol and oral indomethacin/paracetamol combination therapy in the treatment of acute goutlike arthritis: A double-blind, randomized, controlled trial. Ann Emerg Med 2007;49:670-7.
- ^ ab細谷 龍男 「第4章 合併症,併発症に対する治療」、『痛風と核酸代謝』Vol. 26 (2002) No. Supplement pp. 45-57
^ 食品・飲料中のプリン体含有量/公益財団法人痛風財団
^ J Rheumatol 2013 Jun; 40:872.
^ 『高尿酸血症・痛風の治療ガイドライン ダイジェスト版』日本痛風・核酸代謝学会、2002年9月。ISBN 4-901935-02-X。
^ FDAから業者への警告通知
^ USA Todayの記事
関連項目
- 整形外科学
- リウマチ学
- 酸性食品とアルカリ性食品
鶏の尿酸塩沈着症- 偽痛風
外部リンク
尿酸値に潜む死の予言 痛風予備軍が心筋梗塞、NHK「ためしてガッテン」、2013年11月13日
Gout surge blamed on sweet drinks BBCニュース、2008年2月1日、「医者は痛風の患者さんに、砂糖の摂取を減らすように勧めるべきである」(英語)
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||